9. Química orgánica: los compuestos del carbono.
Contenidos
- ¿Por qué una química del carbono? Características de los compuestos del carbono.
- Nomenclatura y formulación de compuestos orgánicos
- Isomería.
- Reactividad de los compuestos orgánicos.
- Tipos de reacciones orgánicas
- Otras reacciones orgánicas
- Obtención y estudio de algunos alcoholes, ácido y ésteres de interés.
- Medicamentos y química orgánica.
- Apuntes que usaremos en clase (Paco)
- Apuntes de orgánica muy claros con indicadiones de petroquímica y polimerización. IDEALES.
- Una presentación bien organizada....
Programa de iniciación a la formulación orgánica
El programa NOMENSET.EXE que ya usamos en clase el pasado curso, es muy sencillo y se puede variar la fórmula con los botones de arriba y abajo, el programa nos va dando el nombre en inglés. Práctico para realizar los primeros pasos de formulación de Química Orgánica. Hay que descargarlo e instalarlo en vuestro ordenador (Windows). Descargar
Prefijos desde C-1 a C-50

Isomería
Tabla de preferencia de grupos funcionales (archivo pdf)


Actividades
Errores habituales de química orgánica
1. Formulación: No encontrar la cadena principal en los ésteres y en las amidas. Acude a la regla de los ojos:

2. En los isómeros geométricos, los átomos con el doble enlace tiene que ser C=C, pero...NO sirven moléculas con una función aldehido o cetona ( C=O ), ni tampoco un C=C cuando en uno de los carbonos tenemos DOS sustituyentes iguales:
- NO SIRVE
- SI SIRVE

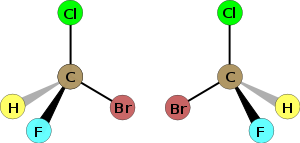
3. En los isómeros ópticos, al menos uno de los átomos de C debe ser asimétrico, es decir, debe estar sustituido por 4 sustituyentes diferentes. No serán carbonos asimétricos aquellas moléculas que tengan enlaces CC (dobles o triples) o enlaces C=O.
Suscribirse a:
Entradas (Atom)